고정밀 데이터 취득 모듈을 사용하여 유세포분석기 설계를 빠르게 구현
DigiKey 북미 편집자 제공
2022-04-21
유세포분석기는 임상의와 진단의가 세포 특성을 분석하는 데 널리 사용되며, 단백질 수준, 혈액 건강, 세분성, 세포 크기 등과 같은 특성을 한 번에 한 세포씩 광학적으로 평가합니다. 유세포분석기는 매우 민감한 시스템이지만, 세포분석기 설계자는 분석 시간을 단축해야 한다는 지속적인 압박을 느끼고 있으므로 유세포분석기와 관련 전자 장치 모두에 대한 새로운 접근 방식이 필요합니다.
세포분석기는 개별 세포에 레이저 광선을 비추어 산란된 형광 신호를 생성합니다. 결과로 제공되는 조명을 빠르고 정확하게 캡처하여 디지털 신호로 변환하려면 애벌런치 광 다이오드(APD)와 복잡한 전자 장치가 필요합니다. 특히, 유세포분석기 데이터 취득 시스템의 정확성을 보장하기 위해 고속 저소음 장치가 필요한 것을 감안하면 이 공정에 대한 회로망을 설계하여 구현하는 데 오랜 시간이 걸릴 수 있습니다.
유세포분석기 분석을 더 빠르고 비용 효율적으로 지원하기 위해 설계자는 내부 증폭기 구동기와 아날로그 디지털 컨버터(ADC)로 구성된 데이터 취득 솔루션을 사용하여 속도 및 정확성 문제를 해결할 수 있습니다.
이 기사에서는 유세포분석기 시스템의 작동 방식을 간략하게 살펴본 다음, 18비트 ADC 모듈인 Analog Devices의 ADAQ23878을 소개하고 이 모듈을 사용하여 유세포분석기 감지 및 변환 단계를 설계하는 방법을 보여줍니다. 또한 관련 평가 키트를 소개합니다.
최신 유세포분석기 원리
최신 유세포분석기는 세포와 표면 분자를 분석하고, 특성을 파악하고, 이기종 세포 집단에서 다양한 세포 유형을 정의하는 자동화된 공정입니다. 1시간이 넘게 걸릴 수 있는 준비 시간을 제외하고 이 기기는 10,000개의 단세포 중 3개~6개 특성 평가를 1분 이내에 수행합니다.
이렇게 하기 위해 유세포분석기의 단세포 준비 단계가 중요합니다. 샘플 집단은 시스 유체에서 유체 역학적으로 발생하여 분석을 위해 단세포계 샘플 스트림으로 세포 또는 미립자의 초점을 맞춥니다. 이 변화로 단세포는 자연 생물학적 특성과 생화학적 성분을 유지해야 합니다.
그림 1은 다중 세포 샘플을 사용하여 위에서부터 시작하는 유세포분석기 기기의 구성도를 보여줍니다.
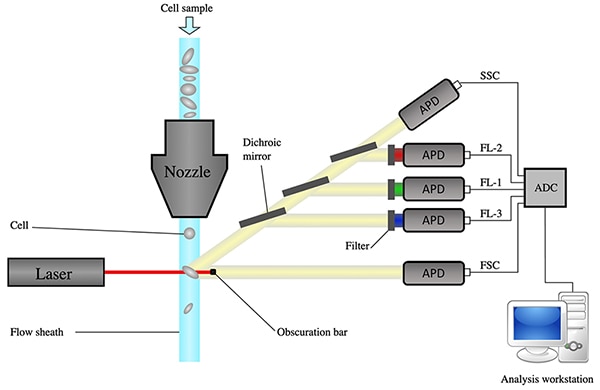 그림 1: 유세포분석기 구성도, 피복부터 데이터 취득으로 초점 이동 (이미지 출처: Wikipedia, Bonnie Baker에 의해 수정됨)
그림 1: 유세포분석기 구성도, 피복부터 데이터 취득으로 초점 이동 (이미지 출처: Wikipedia, Bonnie Baker에 의해 수정됨)
유세포분석기의 6가지 기본 구성 요소는 유세포, 레이저, 애벌런치 광 다이오드(APD), 트랜스 임피던스 증폭기(TIA), ADC 및 데이터 취득 및 분석용 컴퓨터입니다.
유세포분석기에는 유체 흐름 또는 시스 유체가 있으며, 이 유체를 좁혀서 광선을 통해 세포를 전달하고 단일 파일로 정렬합니다. 레이저 광선은 세포를 한 번에 하나씩 캡처하여 전방 산란광(FSC) 신호와 측방 산란광(SSC) 신호를 생성합니다. 형광 광선은 미러와 필터를 통해 정렬된 다음 APD에 의해 증폭됩니다.
다음 단계에서는 APD에 부딪힌 후 결과로 제공되는 광출력을 감지하고 디지털화한 후 분석합니다. 감지의 경우 Analog Devices LTC6268 500MHz 초저 바이어스 전류, 저전압 잡음 FET 입력 연산 증폭기가 감지에 필요한 고속 TIA에 적합합니다.
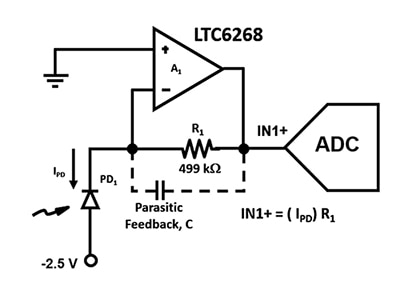 그림 2: TIA 회로에서는 APD(PD1) 및 낮은 입력 전류 FET 연산 증폭기를 사용하여 초저 광 다이오드 전류를 IN1+에서 출력 전압으로 변환합니다. (이미지 출처: Bonnie Baker)
그림 2: TIA 회로에서는 APD(PD1) 및 낮은 입력 전류 FET 연산 증폭기를 사용하여 초저 광 다이오드 전류를 IN1+에서 출력 전압으로 변환합니다. (이미지 출처: Bonnie Baker)
최대한 넓은 대역폭으로 이 증폭기 회로를 설계해야 하므로 기생 정전 용량을 최소화해야 합니다. 예를 들어 기생 피드백 정전 용량 C는 그림 2의 회로 안전성과 대역폭에 영향을 미칩니다. 저항기 패키지 선택에 상관없이 증폭기의 피드백 경로에는 항상 기생 정전 용량이 존재합니다. 하지만 엔드캡 간격이 더 길고 기생 정전 용량이 가장 낮은 0805 패키지는 고속 응용 분야에 더 적합합니다.
R1의 엔드캡 간격을 늘리는 것이 정전 용량을 줄이는 유일한 방법은 아닙니다. 저항 R1 아래에 추가 접지 트레이스를 배치하여 기생 정전 용량을 발생하는 전기장 경로를 차단하여 P2P(Plate-to-Plate) 정전 용량을 줄일 수도 있습니다(그림 3).
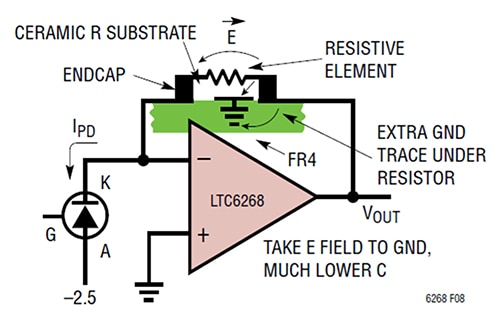 그림 3: 피드백 저항기 아래에 접지 트레이스를 추가하면 전기장이 피드백 측명과 분리되어 접지로 덤핑됩니다. (이미지 출처: Analog Devices)
그림 3: 피드백 저항기 아래에 접지 트레이스를 추가하면 전기장이 피드백 측명과 분리되어 접지로 덤핑됩니다. (이미지 출처: Analog Devices)
특히 이 방법에서는 TIA의 출력 엔드 근처에 있는 저항기 패드 아래와 사이에 짧은 접지 트레이스를 배치합니다. 이 기술에서는 1/(2π*RF*CPARASITIC) TIA 대역폭(11.4MHz)으로 0.028pF의 기생 정전 용량 값을 렌더링합니다.
광학 광신호는 적절한 광학 필터를 통해 여러 애벌런치 다이오드를 지향합니다. APD, TIA 및 ADC 시스템은 이러한 신호를 디지털 표현으로 변환한 후 향후 분석을 위해 데이터를 마이크로 프로세서에 전송합니다.
최신 기기에는 일반적으로 여러 개의 레이저 및 APD가 있습니다. 최신 상업용 장치에는 레이저 10개와 애벌런치 광 다이오드 30개가 있습니다. 레이저 및 광전자 증배관 감지기 수를 늘리면 여러 항체 레이블에서 표현형 마커를 통해 대상 집단을 정밀하게 식별할 수 있습니다.
여전히 분석 속도는 다음 항목의 미세 균형에 따라 달라집니다.
- 유체 피복 속도
- 단세포계를 형성하는 유체 역학적 초점 공정 기능
- 터널 지름
- 세포의 무결성 유지 기능
- 전자 장치
유세포분석기 음향 초점
여러 개의 레이저 및 APD를 추가하면 분석 및 식별이 가속화되지만, 최신 단세포 유세포분석기 방법에서는 기껏해야 분당 최대 100만 개의 개별 셀에 대한 데이터를 수집할 수 있습니다. 대부분의 경우(예: mm당 세포 100개의 낮은 수준으로 혈액에 존재하는 순환 종양 세포 감지) 이는 적합하지 않습니다. 희귀 세포 임상 분야에서 주기적인 테스트를 통해 10억 개 세포를 분석하는 데 많은 시간을 들여야 합니다.
유체 역학 중심 세포 준비 공정의 대안으로 음향 중심 공정이 있습니다. 여기서는 티탄산 지르콘산 납(PZT)과 같은 압전 소재를 유리 모세관에 연결하여 전기 펄스를 기계 진동으로 변환합니다(그림 4a). PZT를 사용하여 사각 유세포의 공진 주파수로 유리 모세관의 측벽을 진동시킴으로써, 시스템에서 다양한 압력 노드 수로 다양한 음향 정재파를 생성합니다.
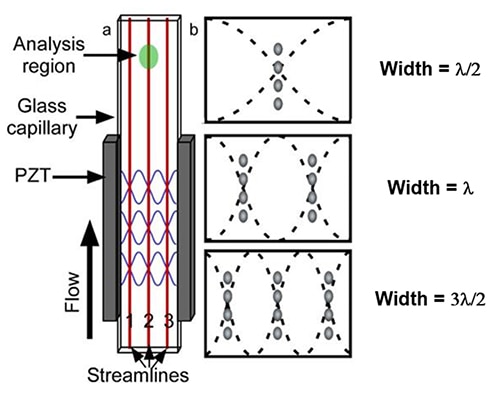 그림 4: 사각 유리 모세관으로 만든 음향 유세포 그림(a). 고정폭 모세관의 처음 세 압력 노드 위치(b). (이미지 출처: National Center for Biotechnology Information)
그림 4: 사각 유리 모세관으로 만든 음향 유세포 그림(a). 고정폭 모세관의 처음 세 압력 노드 위치(b). (이미지 출처: National Center for Biotechnology Information)
이 PZT 주파수 노드는 유동 입자를 여러 개의 개별 유선형으로 정렬합니다(그림 4b). 음향 유세포는 선형 정재파를 사용하여 단일 또는 여러 고조파를 생성함으로써 다양한 파장을 수신합니다. 단순 선형 정재파 모델에서 예측한 대로 샘플 세포는 플로 챔버 내에서 단일 또는 다중 단세포계를 생성합니다.
이렇게 정밀한 세포 구성에서 유체 피복 터널의 폭을 넓혀서 레이저 빔을 통과하는 유속을 높일 수 있습니다(그림 5).
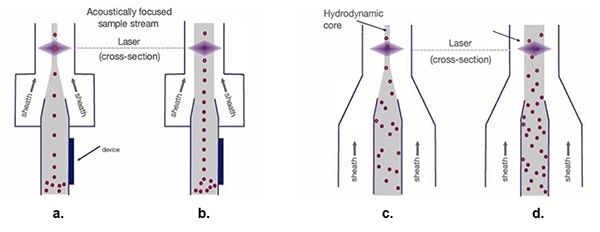 그림 5: 유체 역학적 샘플 스트림에서(c. 및 d.) 피복의 폭을 넓히면 세포 샘플이 산란하여 광학 측정 공정이 어려워집니다. 음향 중심 샘플 스트림(a. 및 b.)에서는 피복의 폭에 상관없이 단일 파일 세포를 유지합니다. (이미지 출처: Thermo Fischer Scientific)
그림 5: 유체 역학적 샘플 스트림에서(c. 및 d.) 피복의 폭을 넓히면 세포 샘플이 산란하여 광학 측정 공정이 어려워집니다. 음향 중심 샘플 스트림(a. 및 b.)에서는 피복의 폭에 상관없이 단일 파일 세포를 유지합니다. (이미지 출처: Thermo Fischer Scientific)
기존 유체 역학 중심 샘플 스트림(그림 5c.)에서는 레이저 스캐닝에 대비하여 단세포계를 배열합니다. 샘플 스트림 코어에 넓은 터널을 사용하면 피복 재료 속도를 높일 수 있지만(그림 5d.) 단세포 구성이 확산되어 신호 편차가 발생하고 데이터 품질이 저하될 수 있습니다.
음향 중심(그림 5a.) 샘플 스트림에서는 넓은 터널에서도 생물학적 세포와 기타 입자를 촘촘하게 배치합니다. 이 정밀 세포 정렬에서는 데이터 품질을 유지하면서 샘플링 속도를 높일 수 있습니다(그림 5b.).
실제로 유세포분석기 음향 초점은 세포 샘플링 주파수를 최대 20배 높여줍니다(그림 6).
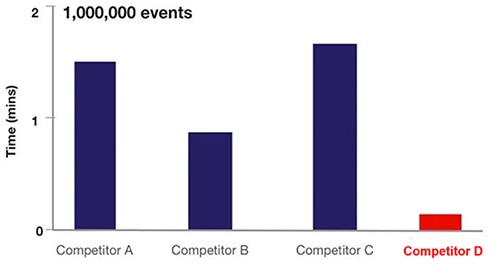 그림 6: 유체 유세포분석기(A, B, C)와 음향 중심 세포분석기(D)를 기반으로 하는 다양한 유세포분석기 장비의 샘플링 속도 비교. (이미지 출처: Thermo Fischer Scientific)
그림 6: 유체 유세포분석기(A, B, C)와 음향 중심 세포분석기(D)를 기반으로 하는 다양한 유세포분석기 장비의 샘플링 속도 비교. (이미지 출처: Thermo Fischer Scientific)
그림 6에서 A, B 및 C 장비는 유체 역학 기술을 사용하고, D 장비는 음향 중심 유세포분석기 흐름 방식을 사용합니다.
음향 중심 유세포분석기 데이터 취득
음향 중심 유세포분석기 장비를 위한 전자 장치를 설계하려면 지름이 큰 노즐을 통과하는 혈액세포 및 시스 유체의 속도를 수용할 수 있는 고속 광 감지 전자 장치가 필요합니다. 앞서 언급한 600MHz 고속 LTC6268은 특수 0805 저항기 패키지 레이아웃과 결합하여 최대 11.4MHz의 광 감지율을 제공합니다(그림 7, 왼쪽). 디지털화를 위해 LTC6268의 출력이 Analog Devices ADAQ23878 ADC에 공급됩니다.
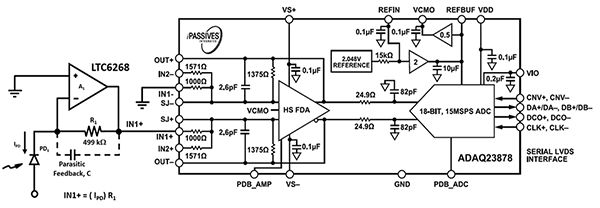 그림 7: ADAQ23878 ADC는 광 다이오드(PD1) 및 TIA 회로(왼쪽)의 광학 신호를 디지털화합니다. (이미지 출처: Bonnie Baker)
그림 7: ADAQ23878 ADC는 광 다이오드(PD1) 및 TIA 회로(왼쪽)의 광학 신호를 디지털화합니다. (이미지 출처: Bonnie Baker)
ADAQ23878은 정밀한 18비트 15MSPS 고속 시스템 인 패키지(SIP) 데이터 취득 솔루션입니다. 설계자의 입력 구동기 소자 선택, 최적화 및 레이아웃 설계 부하를 장치로 전가하여 정밀 측정 시스템의 개발 주기를 단축합니다.
SIP의 모듈식 접근 방식에서는 단일 장치에서 공통되는 여러 신호 처리 및 컨디셔닝 블록을 고속 18비트 15MSPS 연속 근사화 레지스터(SAR) ADC와 함께 결합하여 최종 시스템의 부품 수를 줄입니다. 이러한 블록에는 저잡음 완전 차동 ADC 구동기 증폭기와 안정적인 레퍼런스 버퍼가 포함됩니다.
또한 ADAQ23878은 Analog Devices의 iPassive 기술을 사용하여 온도에 따른 오류 원인을 최소화하고 성능을 최적화하는 중요 수동 부품을 통합합니다. ADC의 빠른 정착 구동기 단계는 빠른 데이터 취득을 보장하는 데 중요한 역할을 합니다.
ADAQ23878 µModule 평가
ADAQ23878을 평가하기 위해 Analog Devices는 EVAL-ADAQ23878FMCZ 평가 기판을 제공합니다(그림 8). 이 기판은 ADAQ23878 μModule의 성능을 보여주며 유세포 분석기 프런트 엔드 설계와 기타 다양한 응용 제품을 평가하는 다목적 도구입니다.
 그림 8: ADAQ23878용 EVAL-ADAQ23878FMCZ 평가 기판은 전원 회로를 탑재하고, 제어 및 데이터 분석을 위한 관련 소프트웨어와 함께 제공되며, SDP-H1과 호환됩니다. (이미지 출처: Analog Devices)
그림 8: ADAQ23878용 EVAL-ADAQ23878FMCZ 평가 기판은 전원 회로를 탑재하고, 제어 및 데이터 분석을 위한 관련 소프트웨어와 함께 제공되며, SDP-H1과 호환됩니다. (이미지 출처: Analog Devices)
EVAL-ADAQ23878FMCZ 평가 기판을 사용하려면 Windows 10 이상을 실행 중인 개인용 컴퓨터, 정밀한 저잡음 신호 발생기, 18비트 테스트에 적합한 대역 통과 필터가 필요합니다. 이 평가 기판에는 ADAQ23878 ACE 플러그인 및 SPD-H1 구동기가 필요합니다.
결론
표준 유체 역학 중심 유세포분석기 기술을 사용하여 생물학적 세포를 한 번에 하나씩 검사하는 데 성공했지만, 빠른 분석을 위해 음향 중심 흐름 방식에 기반하는 기술로 변환되고 있습니다. 하지만 공간, 비용 및 개발 시간을 최소화하면서 고급 유세포분석기를 지원하는 전자 장치를 개선해야 합니다.
위에서 살펴본 바와 같이 LTC6268 고속 연산 증폭기와 정밀한 ADAQ233878 고속 μModule 데이터 취득 솔루션을 결합하여 고급 유세포분석기 장비를 위한 완벽한 데이터 취득 시스템을 구축할 수 있습니다.

면책 조항: 이 웹 사이트에서 여러 작성자 및/또는 포럼 참가자가 명시한 의견, 생각 및 견해는 DigiKey의 의견, 생각 및 견해 또는 DigiKey의 공식 정책과 관련이 없습니다.


